电位滴定法测定酱油中氨基酸态氮的含量
电位滴定法测定酱油中氨基酸态氮的含量
一、实验原理
根据氨基酸的两性作用,加入甲醛以固定氨基的碱性,使羧基显示出酸性,将酸度计的玻璃电极及甘汞电极(或复合电极)插入被测液中构成电池,用碱液滴定,根据酸度计指示的pH值判断和控制滴定终点。
二、仪器与试剂
1、仪器 酸度计 磁力搅拌器 烧杯(250mL) 微量滴定管
2、试剂 pH=6.18标准缓冲溶液;20%中性甲醛溶液;0.05mol/L左右的NaOH标准溶液
三、实验操作方法
(1)样品处理
先根据实验四测出待测酱油的比重,然后吸取酱油5.00mL于100mL容量瓶中,加水定容。吸取定容液20.00mL于250mL烧杯中,加水60mL,放入磁力转子,开动磁力搅拌器使转速适当。用pH6.18的标准缓冲液校正好酸度计,然后将电极清洗干净,再插入到上述酱油液中,用NaOH标准溶液滴定至酸度计指示pH8.2,记下消耗的NaOH溶液体积。
(2)氨基酸的滴定
在上述滴定至pH8.2的溶液中加入10.00mL的中性甲醛溶液,再用NaOH标准溶液滴定至pH9.2,记下消耗的NaOH溶液体积。
(3)空白滴定
吸取80mL蒸馏水于250mL的烧杯中,用NaOH标准溶液滴定至pH8.2,然后加入10.00mL中性甲醛溶液,再用NaOH标准溶液滴定至pH9.2,记下加入甲醛后消耗的NaOH溶液体积。
四、实验计算
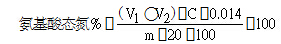
式中:
V1――酱油稀释液在加入甲醛后滴定至pH9.2所用NaOH标准溶液的体积mL;
V2――空白滴定在加入甲醛后滴定至pH9.2所用NaOH标准溶液的体积mL
C ――NaOH标准溶液的浓度mol/L
M――吸取的酱油的质量g
0.014――氮的毫摩尔质量g/m mol
最新消息
- 1赛多利斯新品Practum系列天平
查看次数:1283079......
- 22014年中国和世界十大科技进

由中国科学院、中国工程院主办,中国科学院院......
- 3天美中国与国家纳米科学中心

5月29日下午,天美(中国)科学仪器有限公司与......
- 4分析天平应该如何选砝码以及

查看次数:1107677 分析天平应该如何选砝......
- 5电子天平的使用与维护方法

电子天平是最新一代的天平,是根据电磁力平衡......
