�����ܵ����IJⶨ
�����ܵ����IJⶨ
����
����һ���л�����
��������ԭ��
�����ڴ����������£�Ũ������ȷֽ⻯�ʣ�ʹ��ȫ��ת��Ϊ�����(NH4)2SO4����ȡ����Һ����Һ�ڼ�������������ʹ��������������Һ�У��ñ���ζ���
������������
����������
����ȷ��ȡ����0.5000-1.0000g(��Ʒ��ȡ�������е�Ԫ�غ�����һ�㵪Ԫ����30-50mg֮��Ƚ�����)���������У��������(����أ�����ͭ=15��1)3.2g���ټ���Ũ����10ml������������420�棬ע��۲죬����Ʒ����Ӧ��ͣ���ȣ�����ȴ���ٻ������ȡ�����������Һ��������ɫ��Һ�壬��������0.5-1h��
��������������õ���Ʒ��Hanonȫ�Զ����϶����ǻ��߰��Զ����϶����ǽ�������
�����۵ζ����������յİ���Һ�ñ�����ζ�����Һ��ɫ������ɫ��Ϊ�ƺ�ɫ��Ϊ�յ㡣ͬʱ���հ����顣��ʹ��ȫ�Զ����϶����ǽ����Զ��ζ������ݵζ������ĵı��������������Ʒ�ĺ�������
�����ܼ��㣺N%= (V-V0)��M��1.401/W
����ʽ�У�
����V ���ζ��������ĵı��������ml��
����V0 ���հ��������ĵı��������ml��
����M ����������Һ��Ũ��mol/L��
����W ��������Ʒ������g��
�����������̬���ĵ�����
����������Ʒһ�㶼������ˮ�����ڼ��Խ���������ʹ���ݳ���Ȼ�����������գ�������ζ��������������������������������
�����������裺
������ȡ������Ʒ0.5000��1.0000g(��Ʒ��ȡ�������е�Ԫ�غ�����һ�㵪Ԫ����30-50mg֮��Ƚ�����)���������У���10-20ml����ˮ�ܽ�Ӽ����ζ������㡣
����������������̬���IJⶨ(Zn-FeSO4���Խ��ʻ�ԭ������)
��������ԭ����
������ǿ������Һ�У�п�������������������⣬������̬����ԭΪ������̬����ͬʱҲ��������ԭΪ�ͼ�����ʹ�����ܶ���ʼ�ش��ڡ���������̬��������̬����ԭΪ�����ڻ�ԭ��ͬʱ������İ����������գ�������ζ���������̬������������Ҫ��Ӧ���£���
����FeSO4+2NaOH��Fe(OH)2��+Na2SO4
����8Fe(OH)2+NaNO3+6H2O��8Fe(OH)3+NaOH+NH3��
����Zn+2NaOH��Na2ZnO2+H2
����H2+NaNO3��NaNO2+H2O
����6Fe(OH)2+NaNO2+5H2O��6Fe(OH)3+NaOH+NH3��
���������ⶨ�ĵ�ʵ�������̬������̬���������������Ҫ�ֱ�ⶨ�̬������̬���ĺ�����ֻ������������Һ�����������ա��ζ��ģ���Ϊ�̬��;Ȼ��������ƿ�м���п������������ԭ���ٴν����������ա��ζ�����Ϊ��̬����
������������������װ�á��ζ��ܡ�����ƿ�ȡ���
�����Լ���
����(1)п�ۡ�����������ԭ������ȡ��ѧ����������50g��п��10g�ڴ��в��У�һ��ĥϸͨ��60Ŀɸ�����Ⱥ�������ɫĥ��ƿ�б��á�
����(2)40%����������Һ���ƻ�ѧ����������400g����ˮ�У�ϡ����1������������ƿ�б��á�
����(3)2%������Һ��
����(4) �������ָʾ����
����(5)0.02mol/L��������Һ��
����(6) Һ״ʯ��
�����������裺��ȡ������Ʒ1.1xxg��50ml�ձ��У�������ˮ�ܽ�������ת����100ml����ƿ�У����ݺ�ҡ�ȡ���ȡ����Һ10��20ml(ʹ��������20��30mg����)��250ml����ƿ�У���Zn��FeSO4��ԭ��1.5��3.0g������40%NaOH10ml�����������������ա��ζ���
����������㣺
����N%=(V-V0)��C��0.014/W��100
����ʽ�� V������Һ���ı�����������ml;
����V0���հ����ı�����������ml;
����C���������Ũ�ȣ�mol/L;
����0.014����ԭ�ӵĺ�Ħ��������g/mmol;
����W������10��20ml����Һ�൱��Ʒ��������
�����ġ������е��IJⶨ
��������ԭ����
���������Ǻ�����̬���ĵ��ػ��ʣ����ܼӼ�ֱ�����ɽ���ˮ��Һ����������£�����ˮ����̬����ͬʱ�ݳ�CO2�������ˮ��ķ�ӦʽΪ
����CO(NH2)2+2H2SO4+H2O��2NH4HSO4+CO2��
�������Ӽ����ⶨ�䵪�ĺ�����
�����������Լ���
����ͬ����ȫ���IJⶨ
�����������裺
������ȡ��75���ɵ�������Ʒ0.2xxxg��������ˮ�ܽ������100ml��ҡ�ȱ��á���ȡ�˴���Һ5.00ml��150ml����ƿ�У���Ũ����5ml�������Ļ����ֱ����ȫ��ȥCO2Ϊֹ��Ȼ��������¶�ʹ���ᷢ�̡�ȡ������ȴ����ˮϡ����70��80ml���ٰ�����ȫ���IJ����������ζ�����������
������Ϣ
- 1������˹��ƷPractumϵ����ƽ
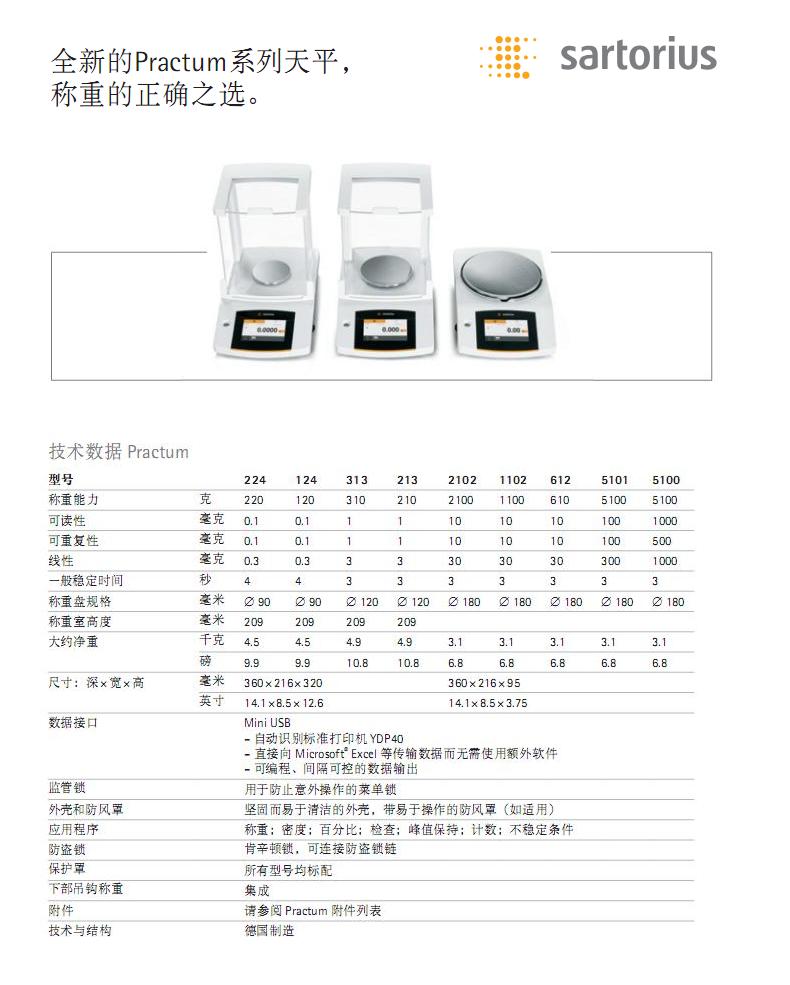
�鿴����:1283079......
- 22014���й�������ʮ��Ƽ���

���й���ѧԺ���й�����Ժ���죬�й���ѧԺԺ......
- 3�����й����������ѧ����

5��29�����磬����(�й�)��ѧ��������˾��......
- 4������ƽӦ�����ѡ�����Լ�

�鿴����:1107677 ������ƽӦ�����ѡ��......
- 5������ƽ��ʹ����ά������

������ƽ������һ������ƽ���Ǹ��ݵ����ƽ��......
